#
Isomérie
On a déjà rencontré la notion de la formule brute d’une molécule. Mais, assez souvent (surtout quand on rencontrera les grosses molécules organiques), on a besoin de plus d’information sur la structure des liaisons covalentes et la forme générale de la molécule. Voici donc trois définitions importantes :
Définition : Formules chimiques
Formule Brute : La formule brute indique les atomes présents dans la molécule et leurs nombres. Exemple :
\text{Butane} \quad \quad\quad C_4H_{10} \quad \quad \quad \quad ; \quad \quad \quad \text{Ethanol }\quad \quad \quad C_2H_6O
Formule développée : Une formule développée fait apparaître l’ensemble des atomes d’une molécule et liaisons covalente qui les relient. Exemple :
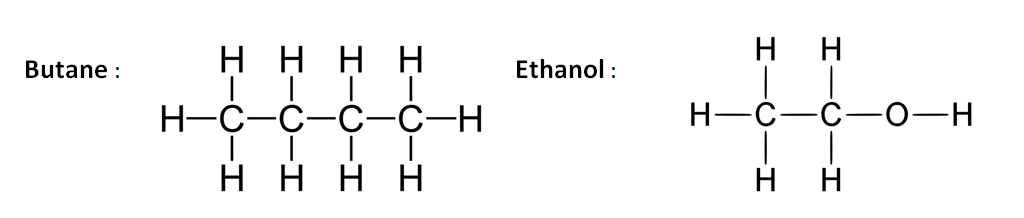
Formule semi-développée : La formule semi-développée n’indique pas les liaisons avec les atomes d’hydrogène. Les symboles de ces atomes sont groupés avec ceux des atomes auxquels ils sont liés. Exemples :
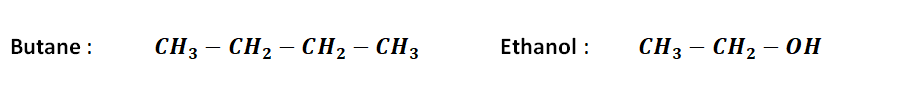
+++ \triangleright \quadExercice . Considérez la formule brute de butane. La formule développée propose ci-dessus, est-elle la seule possible ? +++
Définition : Isomère
Deux molécules sont des isomères si elles ont une même formule brute, mais des enchaînements d’atomes (i.e. formules développées) différents.
